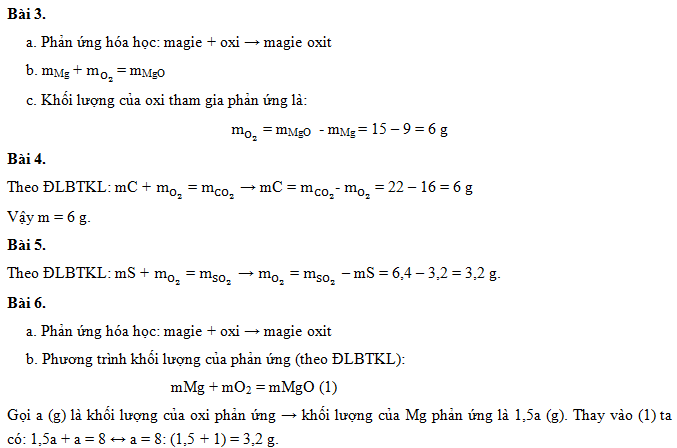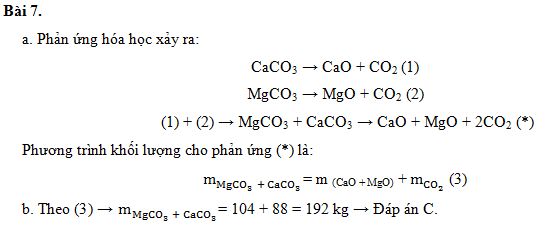Dưới đây là danh sách Bài tập định luật bảo toàn khối lượng hay nhất được tổng hợp bởi chúng tôi
Định luật bảo toàn là một trong những công cụ hữu hiệu nhất giúp giải các bài toán về phép đo phân tích một cách hiệu quả. Bài viết này giúp cung cấp những kiến thức cơ bản về định luật bảo toàn khối lượng cũng như các bài tập vận dụng giúp các em nắm chắc kiến thức hơn.
Luật Bảo tồn Thánh lễ
Tôi. Lý thuyết cần nhớ
1. Định luật bảo toàn khối lượng: “Trong phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
Giả sử phản ứng giữa a + b tạo ra c + d, công thức khối lượng của nó được viết dưới dạng:
ma + mb = mc + md
Ví dụ: Bari Clorua + Natri Sulfat Bari Sulfat + Natri Clorua. Chất lượng của nó là:
Bari clorua + natri sunfat = Bari sunfat + natri clorua
2. Áp dụng: Trong một phản ứng với n loài, nếu biết khối lượng của (n-1) loài thì có thể tính được khối lượng của các loài còn lại.
Hai. Ứng dụng Thực hành
Đăng 1.
A. Phát biểu định luật bảo toàn khối lượng
b. Giải thích tại sao khối lượng của vật chất được bảo toàn trong các phản ứng hóa học?
bài 2. Trong phản ứng hóa học: bari clorua + natri sunfat bari sunfat + natri clorua . có nghĩa là khối lượng của natri sunfat na2so4 là 14,2g, và khối lượng của bari sunfat và natri clorua nacl tương ứng là 23,3g và 11,7g.
Tính khối lượng bari clorua bacl2 phản ứng
Bài 3. Đốt cháy hết 9 g m gam magie kim loại trong không khí thu được 15 g hỗn hợp magie oxit. Biết rằng magie cháy xảy ra do phản ứng với oxi o2 trong không khí.
A. Viết phản ứng hóa học trên.
b. Viết công thức khối lượng để phản ứng xảy ra.
c. Tính khối lượng các loại oxi đã phản ứng.
Bài 4. Cần 16 gam oxi để đốt cháy m (g) cacbon để tạo ra 22 gam cacbon đioxit. Tính m
Bài 5. Đốt 3,2 gam lưu huỳnh trong không khí tạo ra 6,4 gam lưu huỳnh đioxit. Tính khối lượng oxi đã phản ứng.
Bài 6. Đốt cháy m gam magie kim loại trong không khí thu được 8g hợp chất magie oxit (mgo). Biết rằng khối lượng magie tính theo mg tham gia phản ứng gấp 1,5 lần khối lượng oxi (không khí).
A. Viết các phản ứng hóa học.
b.Tính khối lượng của phản ứng giữa miligam và oxi.
bài 7. Dolomit (hỗn hợp của caco3 và mgco3), khi nung nóng, loại đá này tạo ra 2 oxit là canxi oxit cao và magie oxit mgo, tạo ra khí cacbonic.
A. Viết các phản ứng hóa học và phương trình khối lượng xảy ra khi đốt cháy đôlômit.
b.Nếu nung nóng đôlômit thì sau phản ứng thu được 88 kg khí cacbonic và 104 kg hỗn hợp hai oxit, khối lượng của đôlômit phải là:
A. 150 kg b. 16 kg c. 192 kg Kết quả khác.
Bài 8. Giải thích tại sao khi nung nóng thanh sắt thì khối lượng thanh tăng lên còn khi nung nóng thanh sắt thì khối lượng lại giảm đi.
bài 9. Hòa tan canxi cacbua (cac2) vào nước (h2o) thu được khí axetilen (c2h2) và canxi hiđroxit (ca (ồ) 2).
A. Lập phương trình khối lượng cho quá trình trên.
b. Nếu bạn sử dụng 41 g cac2, bạn nhận được 13 g c2h2 và 37 g ca (oh) 2. Vậy nên dùng bao nhiêu ml nước? Biết rằng khối lượng riêng của nước là 1 g / ml.
bài 10. Khi cho m gam X phản ứng với axit clohiđric thì khối lượng magie clorua (mgcl2) nhỏ hơn tổng khối lượng m gam axit clohiđric tham gia phản ứng. Điều này có tuân theo định luật bảo toàn khối lượng không?
bài 10. Khi cho m gam phản ứng với dung dịch hcl thì khối lượng của m gamcl2 nhỏ hơn tổng khối lượng của m gam và hcl. Điều này có tuân theo định luật bảo toàn khối lượng không? giải thích.
Giải pháp
Đăng 1.
A. “Trong một phản ứng hóa học, tổng khối lượng của các sản phẩm bằng tổng khối lượng của các chất phản ứng”
b Giải thích: Trong phản ứng hóa học, liên kết giữa các nguyên tử thay đổi. Chỉ có các electron tham gia vào sự thay đổi này, trong khi số nguyên tử của mỗi nguyên tố không đổi, và khối lượng nguyên tử không đổi. Vì vậy, khối lượng của vật chất được bảo toàn.
Đăng 2.
Áp dụng định luật bảo toàn khối lượng (btkl)
Bari clorua + natri sunfat = Bari sunfat + natri clorua
Đăng 8.
Khi nung nóng thanh sắt, khối lượng tăng lên vì ở nhiệt độ cao thanh sắt phản ứng với oxi tạo thành oxit sắt.
Khối lượng đá vôi giảm khi nung nóng, vì khi nung đá vôi sinh ra vôi sống và khí cacbonic (khí cacbonic là khí dễ thoát ra ở nhiệt độ cao), chỉ còn lại vôi sống nên thể tích nhỏ hơn ban đầu. .
Tất cả nội dung bài viết. Vui lòng xem thêm và tải xuống các tệp chi tiết sau:
Tải xuống
Bài tập trắc nghiệm Hóa học lớp 8 – Xem ngay